Care sunt elementele din corpul uman?
 Share
Share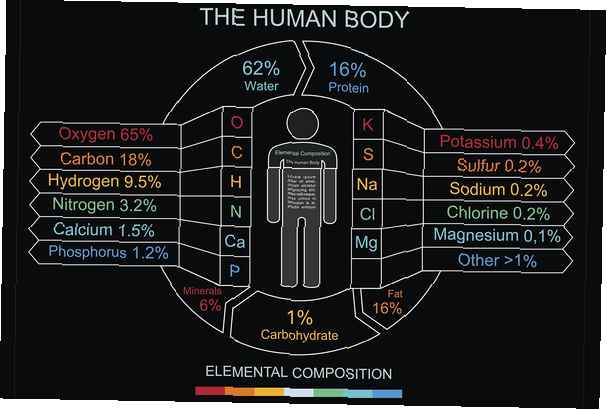
Există mai multe moduri de a lua în considerare compoziția corpului uman, inclusiv elementele, tipul de moleculă sau tipul de celule. Cea mai mare parte a corpului uman este formată din apă, H2O, cu celule constând din 65-90% apă în greutate. Prin urmare, nu este surprinzător faptul că cea mai mare parte a masei corpului uman este oxigenul. Carbonul, unitatea de bază pentru moleculele organice, vine în al doilea rând. 99% din masa corpului uman este formată din doar șase elemente: oxigen, carbon, hidrogen, azot, calciu și fosfor.
- Oxigen (O) - 65% - Oxigenul împreună cu hidrogenul formează apă, care este solventul primar găsit în organism și este utilizat pentru reglarea temperaturii și presiunii osmotice. Oxigenul se găsește în numeroși compuși organici cheie.
- Carbon (C) - 18% - Carbonul are patru locații de legătură pentru alți atomi, ceea ce îl face atomul cheie pentru chimia organică. Lanțurile de carbon sunt utilizate pentru a construi carbohidrați, grăsimi, acizi nucleici și proteine. Ruperea legăturilor cu carbonul este o sursă de energie.
- Hidrogen (H) - 10% - Hidrogenul se găsește în apă și în toate moleculele organice.
- Azot (N) - 3% - Azotul se găsește în proteine și în acizii nucleici care alcătuiesc codul genetic.
- Calciu (Ca) - 1,5% - Calciul este cel mai abundent mineral din organism. Este folosit ca material structural în oase, dar este esențial pentru reglarea proteinelor și contracția musculară.
- Fosfor (P) - 1,0% - Fosforul se găsește în molecula ATP, care este purtătorul de energie primară în celule. Se găsește și în os.
- Potasiu (K) - 0,35% - Potasiul este un electrolit important. Este folosit pentru a transmite impulsurile nervoase și reglarea bătăilor inimii.
- Sulf (S) - 0,25% - Doi aminoacizi includ sulf. Formele de sulf legături ajută la proteine forma de care au nevoie pentru a-și îndeplini funcțiile.
- Sodiu (Na) - 0,15% - Sodiul este un electrolit important. La fel ca potasiul, este utilizat pentru semnalizarea nervilor. Sodiul este unul dintre electroliții care ajută la reglarea cantității de apă din organism.
- Clor (Cl) - 0,15% - Clorul este un ion important (anion) încărcat negativ folosit pentru a menține echilibrul fluidului.
- Magneziu (Mg) - 0,05% - Magneziul este implicat în peste 300 de reacții metabolice. Este folosit pentru a construi structura mușchilor și oaselor și este un cofactor important în reacțiile enzimatice.
- Fier (Fe) - 0,006% - Fierul se găsește în hemoglobină, molecula responsabilă de transportul oxigenului în globulele roșii.
- Cupru (Cu), Zinc (Zn), Seleniu (Se), Molibden (Mo), Fluor (F), Iod (I), Mangan (Mn), Cobalt (Co) - total sub 0,70%
- litiu (Li), Strontium (Sr), Aluminiu (Al), Silicon (Si), Plumb (Pb), Vanadiu (V), Arsenic (As), Brom (Br) - prezente în cantități.
Multe alte elemente pot fi găsite în cantități extrem de mici. De exemplu, corpul uman conține deseori urme de toriu, uraniu, samariu, tungsten, beriliu și radiu. Elementele urmărite considerate esențiale la om includ zinc, iod, eventual siliciu, probabil bor, seleniu, probabil nichel, crom, mangan, litiu, posibil arsenic, molibden, cobalt și, eventual, vanadiu.
Nu toate elementele găsite în corp sunt esențiale pentru viață. Unii sunt considerați contaminanți care par să nu facă niciun rău, dar nu îndeplinesc nicio funcție cunoscută. Exemple includ cesiu și titan. Alții sunt activ toxici, inclusiv mercurul, cadmiul și elementele radioactive. Arsenicul este considerat a fi toxic pentru om, dar servește o funcție la alte mamifere (capre, șobolani, hamsteri) în cantități. Aluminiul este interesant, deoarece este al treilea element cel mai obișnuit în scoarța terestră, dar nu îndeplinește nicio funcție cunoscută în celulele vii. În timp ce fluorul este folosit de plante pentru a produce toxine de protecție, acesta nu servește niciun rol biologic esențial la ființele umane.
De asemenea, poate doriți să vizualizați compoziția elementară a unui corp uman în masă.
surse
- Chang, Raymond (2007). Chimie, Ediția a IX-a. McGraw-Hill. ISBN 0-07-110595-6.
- Emsley, John (2011). Blocurile naturii: un ghid A-Z pentru elemente. OUP Oxford. p. 83. ISBN 978-0-19-960563-7.
- Frausto Da Silva, J. J. R; Williams, R. J. P (2001-08-16). Chimia biologică a elementelor: Chimia anorganică a vieții. ISBN 9780198508489.
- H. A., V. W. Rodwell; P. A. Mayes, Revizuirea chimiei fiziologice, 16 ed., Lange Medical Publications, Los Altos, California 1977.
- Zumdahl, Steven S. și Susan A. (2000). Chimie, Ediția a V-a. Compania Houghton Mifflin. p. 894. ISBN 0-395-98581-1.
