Precipitați definiția și exemplul în chimie
 Share
Share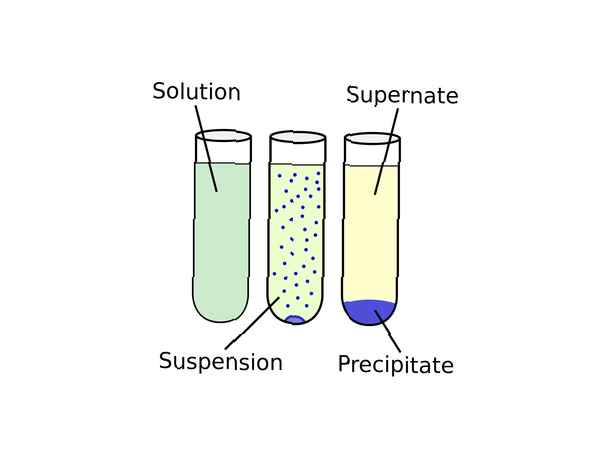
În chimie, a precipita înseamnă a forma un compus insolubil fie prin reacția a două săruri, fie prin modificarea temperaturii pentru a afecta solubilitatea compusului. De asemenea, numele dat solidului care este format ca urmare a unei reacții de precipitare.
Precipitațiile pot indica o reacție chimică, dar poate apărea și dacă concentrația de solutie depășește solubilitatea. Precipitația este precedată de un eveniment numit nucleare, care este atunci când particule mici insolubile se agregă între ele sau formează altfel o interfață cu o suprafață, cum ar fi peretele unui container sau un cristal de semințe.
Cheltuieli cheie: definiția precipitațiilor în chimie
- În chimie, precipitate este atât un verb cât și un substantiv.
- A precipita înseamnă a forma un compus insolubil, fie prin scăderea solubilității unui compus, fie prin reacția a două soluții de sare.
- Solidul care se formează printr-o reacție de precipitare se numește precipitat.
- Reacțiile de precipitare servesc funcții importante. Sunt utilizate pentru purificarea, eliminarea sau recuperarea sărurilor, pentru fabricarea pigmenților și pentru identificarea substanțelor în analiza calitativă.
Precipitate vs Precipitant
Terminologia poate părea un pic confuză. Iată cum funcționează: se numește formarea unui solid dintr-o soluție precipitare. Un produs chimic care determină formarea unui solid într-o soluție lichidă se numește a precipitant. Solidul se numește precipitat. Dacă dimensiunea particulelor compusului insolubil este foarte mică sau nu există o gravitate suficientă pentru a atrage solidul pe fundul recipientului, precipitatul poate fi distribuit uniform în întregul lichid, formând un suspensie. Sedimentare se referă la orice procedură care separă precipitatul de porțiunea lichidă a soluției, care se numește supernatant. O tehnică comună de sedimentare este centrifugarea. După ce precipitatul a fost recuperat, pulberea rezultată poate fi numită "floare".
Exemplu de precipitare
Amestecarea nitratului de argint și clorura de sodiu în apă va determina precipitația clorurii de argint din soluție ca un solid. În acest exemplu, precipitatul este clorura de argint.
La scrierea unei reacții chimice, prezența unui precipitat poate fi indicată urmând formula chimică cu o săgeată în jos:
Ag+ + CI- → AgCl ↓
Utilizarea precipitatelor
Precipitatele pot fi utilizate pentru a identifica cationul sau anionul într-o sare ca parte a analizei calitative. Metalele de tranziție, în special, sunt cunoscute pentru a forma diferite culori ale precipitațiilor, în funcție de identitatea lor elementară și de starea de oxidare. Reacțiile de precipitare sunt utilizate pentru a îndepărta sărurile din apă, pentru a izola produsele și pentru a pregăti pigmenții. În condiții controlate, o reacție de precipitare produce cristale pure de precipitat. În metalurgie, precipitațiile sunt utilizate pentru întărirea aliajelor.
Cum să recuperezi un precipitat
Există mai multe metode utilizate pentru a recupera un precipitat:
Filtrare: În filtrare, soluția care conține precipitatul este turnată peste un filtru. În mod ideal, precipitatul rămâne pe filtru, în timp ce lichidul trece prin el. Recipientul poate fi clătit și turnat pe filtru pentru a ajuta recuperarea. Întotdeauna există o anumită pierdere, fie prin dizolvarea în lichid, trecerea prin filtru, fie prin aderența la mediul de filtrare.
centrifugarea: În centrifugare, soluția este rotită rapid. Pentru ca tehnica să funcționeze, precipitatul solid trebuie să fie mai dens decât lichidul. Precipitatul compactat, denumit peletă, poate fi obținut prin turnarea lichidului. În general, există o pierdere mai mică decât în cazul filtrării. Centrifugarea funcționează bine cu dimensiuni mici de eșantion.
Decantare: În decantare, stratul lichid este turnat sau aspirat departe de precipitat. În unele cazuri, se adaugă un solvent suplimentar pentru a separa soluția de precipitat. Decantarea poate fi utilizată cu întreaga soluție sau în urma centrifugării.
Precipita îmbătrânirea
Un proces numit îmbătrânire precipitat sau digestie are loc atunci când un precipitat proaspăt este lăsat să rămână în soluția sa. De obicei temperatura soluției este crescută. Digestia poate produce particule mai mari cu o puritate mai mare. Procesul care duce la acest rezultat este cunoscut sub numele de maturare Ostwald.
surse
- Adler, Alan D.; Longo, Frederick R.; Kampas, Frank; Kim, Jean (1970). "La prepararea metaloporfirinelor". Journal of Inorganic and Nuclear Chemistry. 32 (7): 2443. doi: 10.1016 / 0022-1902 (70) 80535-8
- Dhara, S. (2007). "Formarea, dinamica și caracterizarea nanostructurilor prin iradierea fasciculului ionic". Recenzii critice în științele materialelor și ale statului solid. 32 (1): 1-50. doi: 10.1080 / 10408430601187624
- Zumdahl, Steven S. (2005). Principii chimice (Ediția a 5-a). New York: Houghton Mifflin. ISBN 0-618-37206-7.
